Unser Erbgut – die DNA – ist der genetische Code in jeder unserer Körperzellen. Sie wird uns von unseren Eltern vererbt und ist in jeder Körperzelle identisch.
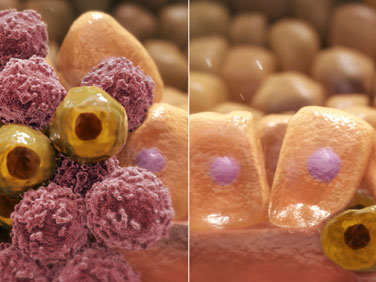
Allerdings haben unsere Zellen viele verschiedene Funktionen: so hat zum Beispiel eine Hautzelle ganz andere Anforderungen und Funktionen als eine Muskelzelle. Wie ist es möglich, dass Zellen mit der gleichen genetischen Information so verschiedene Funktionen ausführen?
Die Antwort liegt in einer zusätzlichen Ebene der Information welche unserer DNA aufliegt. Verschiedene Markierungen an der DNA bestimmen, welche unserer Gene aktiv oder inaktiv sind. Dieser Vorgang wird allgemein als “Epigenetik” bezeichnet. Wenn man sich die DNA als „Hardware“ eines Computers vorstellt, sind epigenetische Markierungen die Software, die bestimmen, welches Programm ausgeführt werden soll.
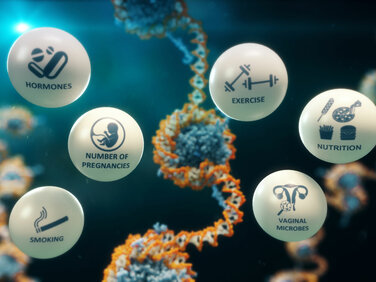
Epigenetische Markierungen, auch als „DNA Methylierung“ bezeichnet, können sowohl von unseren Eltern vererbt werden (wie die DNA selbst), aber auch durch äußere Faktoren beeinflusst werden, zum Beispiel durch die Ernährung, Rauchen, Übergewicht, Aussetzung zu Hormonen oder Chemikalien, und den Alterungsprozess. Dabei integriert die DNA Methylierung die Effekte genetischer (vererbter) und äußerer Faktoren und hinterlässt eine Signatur auf der DNA.
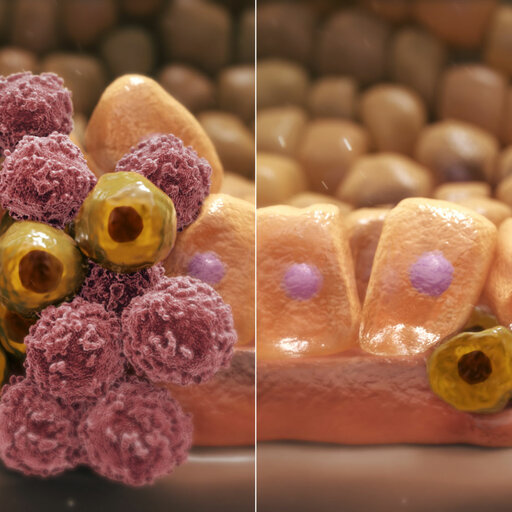
Interessanterweise haben Krebszellen eine bestimmte „Signatur“ der DNA Methylierung, welche oft Jahre vor Krebsentstehung bzw. -diagnose detektiert werden kann. Somit eignet sich die DNA Methylierung zur Krebsrisikovorhersage und/oder Früherkennung. Unsere Forschung deutet darauf hin, dass das individuelle Krebsrisiko durch Untersuchung der DNA Methylierung in einfach zu gewinnenden Proben, zum Beispiel Mundschleimhautabstrichen, Blutproben oder Gebärmutterhalsabstrichproben ermittelt werden kann (siehe FORECEE Projekt).
In unseren zukünftigen Projekten untersuchen wir nun, ob sich diese Markierungen auch dazu eignen, das Risiko über längere Zeiträume hinweg zu überprüfen. In TirolGESUND untersuchen wir den Effekt von vorbeugenden Maßnahmen auf die DNA Methylierung.